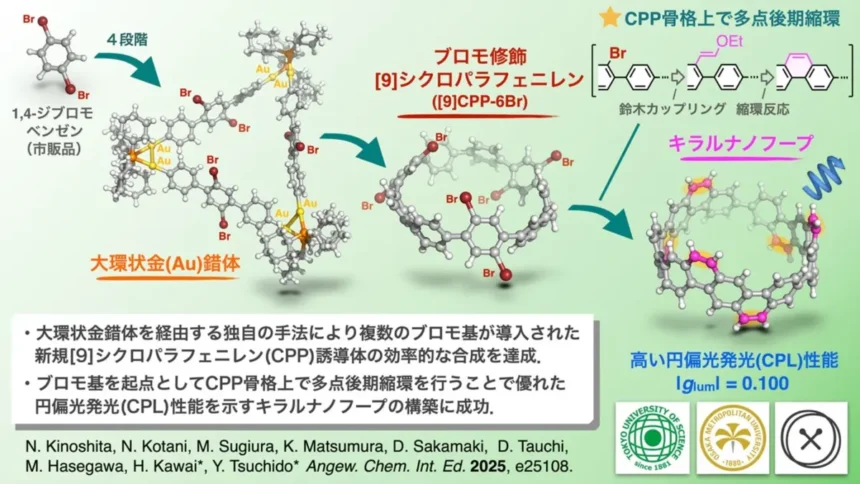
高い円偏光発光を示すキラルナノフープの創製
研究グループは、独自に開発した「大環状金錯体法」を駆使し、6つの臭素原子(ブロモ基)を精密に配置した新規シクロパラフェニレン誘導体([9]CPP-6Br)の効率的な合成を実現しました。
この[9]CPP-6Brを反応点として、多点での鈴木カップリングおよび縮環反応を行うことで、新しいアームチェア型キラルナノフープの構築に成功しました。得られたキラルナノフープは、レアアースなどの希少金属を含む有機金属化合物に匹敵する水準の高い円偏光発光(CPL)性能を示しており、その非対称性因子(|glum|)は0.100という大きな値が観測されています。
本研究は、東京理科大学・大阪公立大学(酒巻 大輔准教授)・北里大学(長谷川 真士教授、田内 大喜助教)の共同研究として行われ、その成果は2025年12月30日に国際学術誌「Angewandte Chemie International Edition」にオンライン掲載されました。
研究の背景と課題
シクロパラフェニレン(CPP)は、ベンゼン環が環状に連結された構造を持つ環状π共役分子であり、湾曲したπ共役系により特異な電子的・光学的性質を示すことで知られています。特に、キラル構造を付与することで円偏光発光(CPL)などのキラル光学特性の精密制御が可能となるため、分子エレクトロニクスや次世代光機能材料、キラル光学デバイスへの応用が期待されています。
しかし、CPP骨格に複数の置換基を精密に導入することは非常に困難でした。特に、分子骨格が完成した後に官能基を導入する「後期修飾」は、多様なπ拡張構造やキラルナノフープを効率的に構築するために重要ですが、既存の合成法では反応性の高い置換基の導入や反応位置の制御が難しく、これがCPPの応用展開を阻む主要な課題となっていました。
本研究グループは、2020年に大環状金錯体を経由する独自のCPP合成法を報告しており、この手法をさらに発展させることで、CPP骨格上の特定位置に6つの臭素原子を精密に配置した[9]CPPの合成に成功しました。
精密に臭素原子を配置した[9]CPP-6Brの合成と特異なリン光特性
研究グループは、独自開発したCPP合成法を用いて、市販の1,4-ジブロモベンゼンを原料とし、大環状金錯体の形成を経由することで、5段階反応で[9]CPP-6Brを高収率(総収率37%)かつサブグラムスケールで合成しました。
![図1. 精密に6つの臭素原子を配置した新規[9]シクロパラフェニレン誘導体([9]CPP-6Br)の合成と光物性](/wp-content/uploads/2026/01/6e68a36c41dc464896499979d3fc94d1.webp)
興味深いことに、合成された[9]CPP-6Brは室温ではほとんど蛍光を示しませんでしたが、液体窒素温度まで冷却すると、623 nm付近に明確なリン光(燐光)が観測されました。これは、6つの臭素原子の導入による重原子効果が項間交差(ISC)を促進し、三重項状態からの放射遷移を可能にしたためと考えられます。このことから、[9]CPP-6Brは後期修飾のための多点反応場としてだけでなく、リン光特性を示す機能性材料としても有用であることが明らかになりました。
後期修飾と高いCPL性能を持つキラルナノフープの構築
[9]CPP-6Brの後期修飾プラットフォームとしての性能を評価するため、パラジウム触媒を用いたクロスカップリング反応が検討されました。その結果、エチニルベンゼンとの薗頭カップリング(57%)、4-メトキシフェニルボロン酸(54%)および(E)-(2-エトキシビニル)ボロン酸ピナコールエステル(72%)との鈴木-宮浦カップリングが効率的に進行し、分子内の全てのブロモ基を一挙に変換できることが示されました。これは、[9]CPP-6Brが多点後期修飾の優れた出発分子であることを示唆しています。
さらに、エトキシエテニル基を導入した多置換CPP誘導体に対して分子内縮環反応を行ったところ、CPP骨格上で同時に6箇所が縮環する多点反応が進行し、新しいキラルナノフープ分子が生成しました。この化合物はアームチェア型構造を持ち、4種類のアトロプ異性体が存在します。
![図2. [9]CPP-6Brを基盤とした後期修飾およびπ拡張によるキラルナノフープ分子の構築](/wp-content/uploads/2026/01/705cfbb70ea031102c27568b6760764f.webp)
これらの異性体をキラルHPLCで分割し、キラル光学特性を評価した結果、D3対称性を持つ異性体において、|glum| = 0.100という非常に大きい非対称性因子を持つ円偏光発光(CPL)が観測されました。この値は、左右の円偏光の強さに約5%の差があることに相当し、一般的なキラル有機分子(|glum|〜0.001)と比較して極めて高い性能です。この成果は、後期π拡張を通じて優れたキラル光学特性を持つナノカーボン分子を創製できる可能性を示しています。
社会的なインパクトと今後の展望
本研究の大きな特徴は、多点修飾可能な[9]CPP-6Brを実験室レベルの設備でサブグラムスケールで合成を可能にした点です。従来、CPPは合成が難しく、特に複数の反応点を精密に配置した誘導体の大量供給は困難でした。この量的制約の解決は、CPPを出発点とした後期修飾化学や機能性材料開発の加速に大きく貢献すると期待されます。
また、本研究で合成されたキラルナノフープが示した非常に高いCPL特性は、次世代ディスプレイ、ホログラフィー、情報暗号化、光学的キラリティーセンシングなど、多岐にわたる応用分野で重要な役割を果たす可能性があります。
今後の展望として、本研究で確立されたCPPの後期π拡張手法により、芳香環の縮環位置や置換基の種類を自在に変化させた多様なナノフープ分子や、より複雑な環状π共役ネットワークの構築が可能になると考えられます。これにより、キラル光学特性のさらなる増強や発光波長のチューニングなど、目的に応じた分子設計が実現することでしょう。将来的には、カーボンナノチューブのボトムアップ型合成への応用にもつながる可能性を秘めています。
研究資金と論文情報
本研究は、科研費基盤研究(C)、科研費学術変革領域(A)高密度共役、徳山科学技術振興財団 研究助成、東京理科大学若手・女性研究者奨励金、人・環境と物質をつなぐイノベーション創出ダイナミック・アライアンスの助成を受けて実施されました。
論文情報
-
雑誌名:Angewandte Chemie International Edition
-
論文タイトル:A Precisely Bromo-Functionalized [9]Cycloparaphenylene as a Platform for Late-stage Multisite π-Extension Toward Chiral Nanohoops
-
著者:Naoya Kinoshita‡, Nanami Kotani‡, Masaya Sugiura, Kotaro Matsumura, Daisuke Sakamaki, Daiki Tauchi, Masashi Hasegawa, Hidetoshi Kawai and Yoshitaka Tsuchido ‡N. KinoshitaとN. Kotaniは等しい貢献度
用語解説
-
シクロパラフェニレン(cycloparaphenylene, CPP)
ベンゼン環がパラ位で環状につながった分子で、カーボンナノチューブの最小構造単位に相当します。湾曲したπ共役系を持ち、特異な電子的・光学的性質を示します。 -
円偏光発光(circularly polarized luminescence, CPL)
右回り・左回りの円偏光を放射する発光現象です。3Dディスプレイ、ホログラフィー、光情報処理、キラルセンシングなどの次世代光学デバイスとして注目されています。 -
後期修飾
分子骨格を完成させた後に特定部位へ官能基を導入する手法です。 -
π拡張
芳香環単位を縮環させ、分子全体のπ電子系を拡げる手法です。光学特性や電子物性が大きく変化するため、機能性材料の設計において重要です。 -
クロスカップリング
金属触媒(主にパラジウム)を用いてハロゲン化芳香族と有機金属試薬を結合させる反応です。鈴木–宮浦カップリングは、有機ホウ素化合物を芳香族ハロゲン化物に結合させる反応で、アリール基やビニル基の導入に広く用いられます。薗頭カップリングは末端アルキンを芳香族ハロゲン化物に結合させる反応で、エチニル基の導入に広く用いられます。 -
glum値(CPL異方性因子)
CPLの偏りの度合いを示す指標で、左円偏光(IL)と右円偏光(IR)の発光強度差を正規化した値です(glum = 2(IL − IR)/(IL + IR))。値が大きいほど円偏光発光の偏りが強く、高性能CPL材料の評価尺度となります。通常のキラル有機分子の多くはglum値が10^-3オーダーですが、本研究で達成した10^-1オーダーという値は有機分子では極めて異例であり、レアアースなどの希少金属を含む有機金属化合物に限られて観測される水準です。